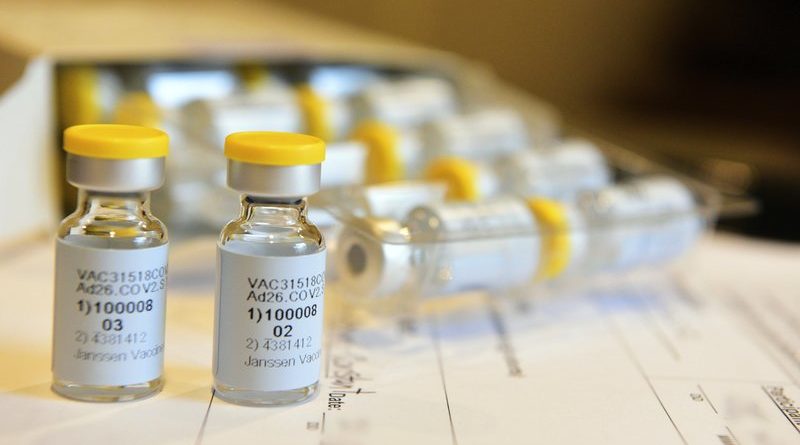
Inicia estudio de última etapa de la primera vacuna de inyección única en EE.UU.
Johnson & Johnson está comenzando un gran estudio final para tratar de probar si una vacuna COVID-19 de dosis única puede proteger contra el virus.
El estudio que comenzará el miércoles será uno de los estudios de vacunas contra el coronavirus más grandes del mundo hasta el momento, probando la vacuna en 60.000 voluntarios en Estados Unidos, Sudáfrica, Argentina, Brasil, Chile, Colombia, México y Perú.
Un puñado de otras vacunas en los EE. UU., Incluidas las inyecciones realizadas por Moderna Inc. y Pfizer Inc., y otras en otros países ya se encuentran en la etapa final de prueba. Hay muchas esperanzas de que las respuestas sobre al menos un candidato que se está probando en los EE. UU. Puedan llegar a fin de año, tal vez antes.
Los funcionarios de salud de EE. UU. Insisten en que la carrera por una vacuna no es escasa.
MÁS SOBRE COVID-19:
– 200.000 muertos mientras Trump vilipendia la ciencia y prioriza la política
– Finlandia despliega perros detectores de coronavirus en el aeropuerto principal
– Contar la historia de COVID: en la ONU, los líderes tejen historias de virus
“Queremos hacer todo lo que podamos sin sacrificar la seguridad o la eficacia, no vamos a hacer eso, para asegurarnos de que terminemos con vacunas que salvarán vidas”, dijo el Dr. Francis Collins, director de los Institutos Nacionales. de Salud, dijo a los periodistas.
Pero muchos especialistas en vacunas se preguntan si la Administración de Alimentos y Medicamentos se apegará a ese objetivo bajo la intensa presión de la administración Trump. El presidente Donald Trump ha presentado constantemente un cronograma más rápido para una nueva vacuna de lo que los expertos dicen que es adecuado para probar completamente a los candidatos.
Trump tuiteó el miércoles el enlace a un informe de noticias sobre el estudio de Johnson & Johnson y dijo que la FDA «debe actuar con rapidez».
Mientras tanto, la prueba de otra vacuna experimental, fabricada por AstraZeneca, permanece en suspenso en los EE. UU. Mientras los funcionarios examinan una cuestión de seguridad, a pesar de que los estudios se han reanudado en otros países.
A principios de esta semana, el vicepresidente Mike Pence instó a los gobernadores estatales a «hacer su parte para generar confianza pública en que será una vacuna segura y eficaz».
Y el Dr. Anthony Fauci, el principal experto en enfermedades infecciosas de EE. UU., Agregó en la llamada a los gobernadores que confía en «un proceso probado y verdadero» que tiene controles y equilibrios integrados, incluida una junta independiente que evalúa el progreso de cada ensayo de vacuna. , así como «la integridad de la FDA».
Estaba previsto que los senadores interrogaran al comisionado de la FDA Stephen Hahn, a Fauci y a otros funcionarios de la administración el miércoles más tarde sobre la respuesta a la pandemia.
Cobertura total: brote de virus
Incluso si la FDA permitiera el uso de emergencia de una vacuna para fin de año, los suministros serían limitados y se entregarían primero a grupos vulnerables como los trabajadores de la salud. Es poco probable que la mayoría de los estadounidenses reciban una vacuna hasta el próximo año.
Los Centros para el Control y la Prevención de Enfermedades quieren que los estados se preparen ahora para implementar las vacunas, lo que presentará enormes desafíos logísticos. El miércoles, los CDC estaban listos para anunciar la distribución de $ 200 millones en fondos aprobados por el Congreso para ayudar a comenzar a establecer operaciones.
El secretario de Salud y Servicios Humanos, Alex Azar, dijo que la campaña de la vacuna COVID-19 se basará en la cooperación de larga data entre el gobierno federal y los estados en materia de inmunizaciones.
La vacuna de J&J está fabricada con una tecnología ligeramente diferente a la de otras en las pruebas de etapa avanzada, siguiendo el modelo de una vacuna contra el ébola creada por la empresa. A diferencia de las otras tres vacunas que comenzaron las pruebas de etapa tardía en los EE. UU., Solo requiere una inyección, no dos. A pesar de un comienzo más tardío de las pruebas que algunos de sus competidores, el Dr. Paul Stoffels, director científico de J&J, dijo a los periodistas que el estudio era lo suficientemente grande como para dar respuestas posiblemente a principios del próximo año.