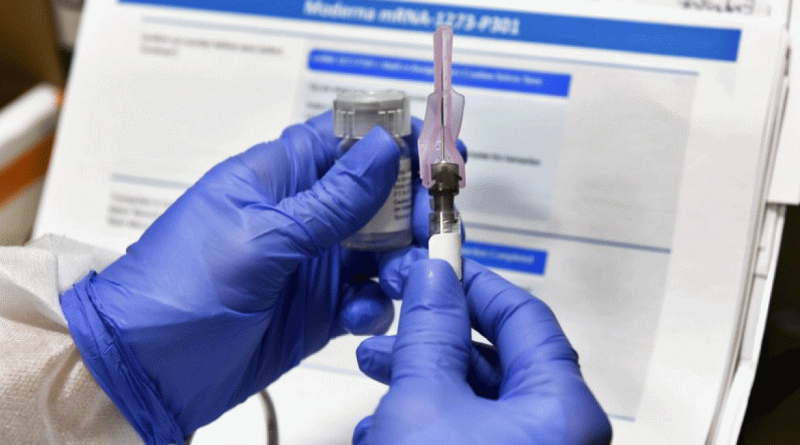
Moderna pide a EEUU y la UE que usen su vacuna de emergencia
AP
Washington Hispanic:
Moderna Inc. se disponía el lunes a pedir a los reguladores de Estados Unidos y de la Unión Europea que permitan el uso de emergencia de su vacuna contra COVID-19, luego de que nuevos resultados confirmaron que ofrece una protección sólida, intensificando la carrera para empezar a administrar las inyecciones mientras la pandemia de coronavirus avanza.
Varias candidatas a vacuna deben tener éxito para que el mundo ponga alto a la pandemia, que ha tomado un segundo aire en Estados Unidos y Europa. Los hospitales estadounidenses han llegado a su límite mientras la nación registra más de 160.000 casos nuevos al día y más de 1.400 decesos diarios. Desde que surgió por primera vez hace un año en China, el virus ha provocado la muerte de más de 1,4 millones de personas en el mundo.
Moderna está detrás de Pfizer y su socia alemana BioNTech en los intentos para empezar a vacunar a la población estadounidense en diciembre. Los reguladores británicos también están evaluando la inyección de Pfizer y otra de la asociación entre Universidad de Oxford y AstraZeneca.
Moderna creó sus dosis con los Institutos Nacionales de la Salud de Estados Unidos y ya había obtenido buenas señales mientras estaba trabajando, pero dijo que obtuvo los resultados finales que necesitaba durante el fin de semana, que muestran que la vacuna tiene una efectividad de más del 94%.
De los 196 casos de COVID-19 involucrados en este enorme estudio, 185 fueron participantes que recibieron placebo y 11 que les administraron la vacuna real. Los únicos que se enfermaron de gravedad 30 participantes, entre ellos uno que falleció— habían recibido vacunas falsas, dijo el médico Tal Zaks, el director médico de la compañía con sede en Cambridge, Massachusetts.
Cuando supo de los resultados, “me permití llorar por primera vez”, comentó Zaks a The Associated Press. “Tan sólo en el ensayo, ya hemos salvado vidas. Imaginen el impacto cuando se multiplique a la gente que pueda obtener esta vacuna”.
Moderna dijo que la efectividad de la vacuna y un buen historial de seguridad, con efectos secundarios temporales parecidos a los síntomas de la influenza, significan que la farmacéutica ha cumplido con los estándares fijados por la Administración de Alimentos y Medicamentos de Estados Unidos (FDA por sus siglas en inglés) para un uso de emergencia antes de que se finalice la etapa final de pruebas. La Agencia Europea de Medicamentos ha señalado que también está dispuesta a dar una autorización “condicional”.
La FDA ha prometido que antes de que decida desplegar cualquier vacuna contra el COVID-19, sus asesores científicos debatirán públicamente si hay suficiente evidencia detrás de cada candidata a vacuna.
El Departamento de Salud y Ciencia de The Associated Press recibe el apoyo del Departamento de Educación Científica del Instituto Médico Howard Hughes. La AP es la única responsable de todo el contenido.